Caso Clínico
Desafíos diagnósticos y terapéuticos en un caso de leiomiomatosis parasitaria, metastatizante y peritoneal diseminada: un abordaje complejo
1Hospital Universitario Miguel Servet, Zaragoza, España
2Hospital Universitario Virgen de las Nieves Granada, España
Se describe un caso que presenta una rara combinación de leiomiomatosis parasitaria, metastatizante y peritoneal diseminada, desafiando el diagnóstico y tratamiento. La paciente presentó síntomas relacionados con la compresión de estructuras pélvicas inicialmente, seguidos de la aparición de leiomiomas en la pared abdominal y finalmente de leiomiomas distribuidos por el peritoneo que terminaron asociando ascitis. El diagnóstico diferencial es amplio y complejo e incluye las metástasis de tumores primarios, entre otros. Además, la falta de un estándar de tratamiento subraya la complejidad de estas patologías, abogando por un enfoque quirúrgico integral y considerando las opciones de tratamiento farmacológico si existe deseo gestacional.
Palabras clave: Leiomiomatosis; Diagnóstico diferencial; Cirugía
Introducción
Los leiomiomas (también denominados miomas o fibromas) son los tumores pélvicos más frecuentes en mujeres y su prevalencia se incrementa durante la edad reproductiva. En ocasiones, los leiomiomas tienen un patrón de crecimiento agresivo de localización extrauterina, siendo su manifestación significativamente rara, con pocos casos descritos en la bibliografía. Estas patologías con crecimiento atípico son la leiomiomatosis peritoneal diseminada, la leiomiomatosis metastatizante, la leiomiomatosis intravascular, la leiomiomatosis parasitaria, los leiomiomas disecantes y la leiomiomatosis retroperitoneal1.
Presentamos un caso excepcional y único en la literatura científica que combina la presentación en forma de leiomiomatosis peritoneal diseminada, metastatizante y parasitaria, asociando ascitis.
Comunicación del Caso
Se describe el caso de una paciente mujer de 40 años en seguimiento en las consultas del servicio de ginecología y obstetricia por historia clínica de leiomiomatosis extrauterina. En 2016, la paciente presentó clínica de pesadez pélvica y dolores esporádicos, diagnosticándose entonces una masa polilobulada de 10 cm de diámetro, vascular, de aspecto miomatoso, con base de implantación en cara superior vesical sin contacto con el útero compatible con mioma parasitario, que fue resecado en quirófano con anatomía patológica intraoperatoria y definitiva de leiomioma atípico sin signos de malignidad (atipia nuclear leve-moderada, sin necrosis e índice proliferativo (Ki67 inferior al 5%). En el mismo acto quirúrgico, se resecó dos miomas subserosos uterinos de pequeño tamaño y otro en la trompa uterina derecha de 2 cm de diámetro.
En 2020, y tras controles evolutivos favorables, la paciente ingresó en el programa de reproducción asistida por infertilidad primaria y deseo gestacional. En septiembre de 2021, se realizó fecundación in vitro consiguiendo gestación. Durante los controles gestacionales ecográficos se objetivó lesiones sólidas parauterinas bilaterales heterogéneas, sin morfología típica de miomas, por lo que se solicitó resonancia pélvica en mayo de 2022 (28s+4 de gestación). En ella se visualizó múltiples lesiones nodulares y nódulos superficiales contiguos en pared abdominal de similares características a la lesión intrapélvica extrauterina de 2016. Se realizó estudio anatomopatológico de la lesión de la pared abdominal, con resultado de leiomioma típico, por lo que se continuó con la gestación con parto a término eutócico.
La paciente acudió a urgencias posteriormente por episodios recurrentes de ascitis con citología negativa del líquido, realizándose tomografía en enero de 2023 y se objetivó crecimiento de los nódulos catalogados previamente como leiomiomas, distribuidos por la cavidad abdominal. Tras biopsia y resultado negativo de malignidad, se decidió en sesión multidisciplinar la exéresis de los implantes peritoneales accesibles, histerectomía y doble anexectomía (inducción de menopausia quirúrgica), que se realizó en febrero.
La cirugía se llevó a cabo mediante un abordaje con laparotomía media y colaboración con el servicio de cirugía general, quienes realizaron la resección de una gran masa (8 a 10 cm) en fosa iliaca derecha-flanco derecho, y otras de menor tamaño de distribución difusa intraabdominal. En la pelvis se objetivó un útero aumentado de tamaño polimiomatoso, con mioma dominante en parametrio derecho, subseroso de unos 6 cm. Se palpó otros miomas intramurales de menor tamaño y 2 subserosos en el fondo uterino cara anterior, de 2 cm. Los anejos eran de aspecto normal. Se visualizó también varices en vasos pélvicos parametriales y paracervicales. Se procedió a realizar histerectomía y doble anexectomía y cierre por planos.
Posteriormente, en nueva sesión multidisciplinar y tras conocer el resultado de leiomiomatosis sin signos de malignidad, se decidió no instaurar tratamiento médico hormonal y realizar seguimiento estrecho. Hasta la fecha la paciente únicamente presenta clínica asociada a la menopausia quirúrgica, sin recibir terapia hormonal sustitutiva por sus antecedentes.
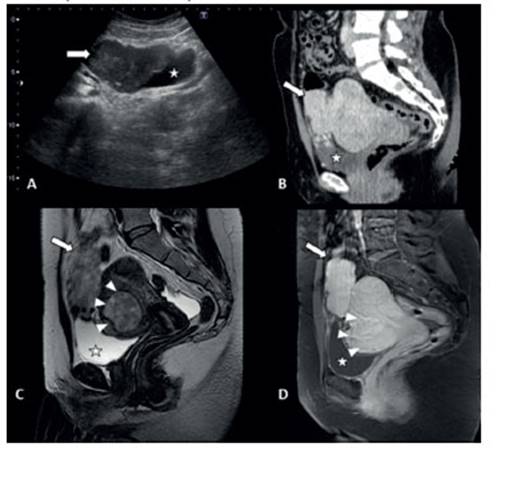
Figura 1 Leiomiomatosis parasitaria. a) ecografía abdominal. se visualiza una masa heterogénea (flecha) localizada en el plano superior a la vejiga (estrella). b) tomografía con contraste en corte sagital. se confirma la presencia de la masa (flecha) de localización supravesical (estrella), adyacente al útero polimiomatoso. c) resonancia potenciada en t2 en corte sagital. la masa (flecha) impronta sobre el útero, sin una clara relación de dependencia con el mismo. además, presenta una señal hipointensa y heterogénea, similar a uno de los miomas uterinos (cabezas de flecha). d) resonancia potenciada en t1 con supresión grasa, tras la administración de contraste. la masa (flecha) presenta el mismo realce que el útero y el mioma uterino (cabezas de flecha).
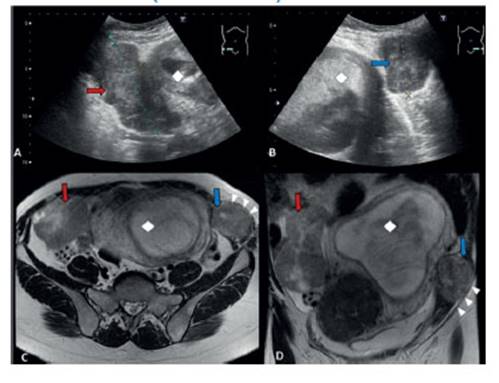
Figura 2 Leiomiomatosis metastatizante. a y b) ecografía abdominal. se visualizan dos masas heterogéneas (flecha roja y azul) a ambos lados del útero gestante (rombo). c y d) resonancia potenciada en t2, cortes axial y coronal. se confirma la presencia de una masa en la región parauterina derecha (flecha roja), y otra masa en la pared abdominal izquierda (flecha azul), delimitada por la fascia del oblicuo externo (cabezas de flecha).
Discusión
La leiomiomatosis parasitaria se define por la aparición de miomas cuya vascularización es independiente de la arteria uterina y que se localizan en estructuras adyacentes al útero, en nuestro caso en la cara superior de la vejiga. Estas lesiones pueden ejercer efecto de masa comprimiendo estructuras pélvicas como la uretra, el cuello vesical o el uréter, provocando urinaria obstructiva clínica, y aunque en nuestro caso la sintomatología urinaria no era significativa, sí lo era la sensación de ‘pesadez’, tal y como lo refería la paciente inicialmente. Esto llevó inicialmente a su descubrimiento, tras la realización de pruebas radiológicas y a la confirmación mediante cirugía y estudio de la pieza quirúrgica1.
Por otro lado, la leiomiomatosis metastatizante es una entidad de la cual se han publicado escasos 150 casos en la literatura científica y se caracteriza por la aparición de múltiples leiomiomas en localizaciones distantes del útero, afectando más frecuentemente a los pulmones. La afectación del corazón, el cerebro, los ganglios linfáticos, el hueso y la piel es menos habitual. Una de las particularidades de este caso es que no se localizaron otros leiomiomas más allá de aquellos en el tejido subcutáneo/piel de la pared abdominal, un sitio ya de por sí raro según la bibliografía. Además, creemos que ninguna de las dos teorías más comúnmente aceptadas concuerda con nuestro caso, pues la hipótesis de la diseminación hematógena no explicaría la no existencia de otros leiomiomas a distancia, y la teoría de transformación metaplásica tampoco explicaría la presencia de estos en escaso número en la pared abdominal1.
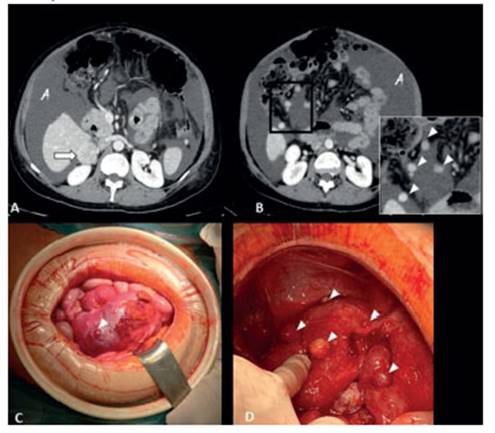
Figura 3 Leiomiomatosis metastatizante y peritoneal diseminada. a) tomografía con contraste en corte axial. se evidencia una masa metastásica en la glándula suprarrenal derecha (flecha), con realce homogéneo. también se visualiza ascitis (letra ‘a’). b) tac con contraste en corte axial. en cortes mesogástricos se detectan pequeños implantes en la cavidad peritoneal (cabezas de flecha). c y imágenes quirúrgicas. se confirma la presencia de los implantes peritoneales durante el procedimiento quirúrgico (cabezas de flecha).
Por otra parte, la leiomiomatosis peritoneal diseminada es una patología benigna que se caracteriza por el crecimiento de múltiples nódulos de tejido muscular liso en el peritoneo abdominal (desde unos pocos milímetros hasta 5 a 10 cm)1,2). Fue descrita por primera vez por Wilson y Peale, en 1952, y posteriormente fue reconocida como una entidad distinta por Taubert y col. en 19652. Al igual que con la leiomiomatosis metastatizante, la etiología y la fisiopatología de esta enfermedad no están claras, existiendo tres teorías: la hormonal, la genética y la iatrogénica. En nuestro caso particular, la teoría hormonal sería la que mejor explicaría la evolución de esta paciente y la aparición de esta entidad tras la sobreestimulación hormonal que conllevó primero una FIV y posteriormente la gestación. Asimismo, existe en la literatura varios casos que refuerzan nuestra posición hormonal3. A pesar de los antecedentes quirúrgicos, no creemos que la teoría iatrogénica explique nuestro caso.
El diagnóstico de estas patologías es complejo y a menudo requieren de biopsia o estudio de la pieza quirúrgica, ya que no existe una presentación patognomónica en la imagen radiológica. El principal diagnóstico diferencial es el de metástasis de un tumor primario maligno oculto, ya sea en el caso de la leiomiomatosis metastatizante como de la leiomiomatosis peritoneal diseminada. En esta última enfermedad, el diagnóstico diferencial es incluso más amplio entre los que se incluyen el mesotelioma peritoneal primario, linfomas, tuberculosis y tumores dermoides1-3.
Actualmente sigue siendo dudoso que se produzca una transformación maligna, existiendo casos aislados en la literatura, siendo la ascitis y los antecedentes de atipia nuclear en nuestra paciente un signo de alerta. La transformación se caracteriza por atipia nuclear citológica, necrosis tumoral, crecimiento infiltrativo y aumento de la actividad mitótica3,4. Por otra parte, no existe una pauta de tratamiento estándar para la leiomiomatosis peritoneal diseminada ni metastatizante. Algunos autores recomiendan la cirugía inicial con debulking (reducción de volumen) peritoneal e histerectomía/ovariectomía, mientras que otros piensan que la cirugía extensa solo debe considerarse en casos de compresión orgánica, siendo precedida por terapia hormonal administrada de manera neoadyuvante5. En este sentido, se ha observado regresión espontánea de los nódulos peritoneales después del parto en algún caso aislado. Sin embargo, la clínica particular de nuestra paciente no permitió este abordaje, ya que tras el parto se sucedieron múltiples episodios de ascitis con empeoramiento de la clínica.
En cuanto al tratamiento médico, no está claro el papel de los agonistas de la hormona liberadora de gonadotropina que teóricamente reduciría el tamaño de los nódulos, puesto que se ha comunicado un caso que describió la estimulación paradójica de estos tumores después del tratamiento3,6. Por su parte, el tamoxifeno ha demostrado ser eficaz in vitro, pero su papel sigue siendo incierto in vivo, mientras que el raloxifeno se documentó como un tratamiento exitoso cuando se administró solo en mujeres posmenopáusicas o en asociación con un inhibidor de aromatasa, con resultados mixtos en mujeres premenopáusicas6. La quimioterapia sistémica con doxorrubicina y dacarbazina se podría considerar como una opción de tratamiento para situaciones irresecables o enfermedad metastásica.
Respecto al tratamiento quirúrgico, los abordajes laparoscópicos han transformado el manejo de los leiomiomas, permitiendo procedimientos menos invasivos y una recuperación más rápida. Sin embargo, en casos atípicos y con enfermedad tan extendida y voluminosa, como el presentado, se requiere un diagnóstico más preciso y, a menudo, estudios patológicos definitivos mediante el análisis de piezas quirúrgicas7-10. En nuestra paciente creemos que el abordaje quirúrgico (histerectomía y doble anexectomía junto con la resección del mayor número posible de miomas intraabdominales) fue el más seguro, tanto a corto como a largo plazo, ya que la paciente no tenía mayor deseo gestacional y la menopausia quirúrgica debería mejorar los síntomas y reducir la progresión de la enfermedad.
Por último, hay que mencionar que los avances en inteligencia artificial ofrecen nuevas perspectivas en el diagnóstico por imagen y la interpretación de datos clínicos, lo que podría mejorar la identificación y caracterización de casos complejos de leiomiomas. En este contexto, la combinación de abordajes laparoscópicos y tecnologías de inteligencia artificial representa una dirección prometedora para el manejo de leiomiomas, especialmente en casos complejos como el presentado.
Referencias Bibliográficas
1. Martínez-Cachero García M, Menéndez de Llano Ortega R, Martínez Camblor L, Carrasco Aguilera B, Rodríguez Castro J, Gómez Illán R. Leiomiomatosis extrauterina, la gran simuladora. Radiologia. 2023;65(3):251-7. doi: 10.1016/j.rx.2023.01.002 [ Links ]
2. Rosati A, Vargiu V, Angelico G, Zannoni GF, Ciccarone F, Scambia G, et al. Disseminated peritoneal leiomyomatosis and malignant transformation: A case series in a single referral center. Eur J Obstet Gynecol Reprod Biol. 2021;262:21-7. doi: 10.1016/j.ejogrb.2021.05.006 [ Links ]
3. De Vos T, Weyers S, Braems G, Villeirs G, Lambein K, Makar A, et al. Leiomyomatosis peritonealis disseminata associated with ascites and endometriosis: a case report and review of the literature. Acta Chir Belg. 2013;113(5):357-63. doi: 10.1080/00015458.2013.11680945 [ Links ]
4. Zyla MM, Dzieniecka M, Kostrzewa M, Stetkiewicz T, Wilamowska A, Ksiezakowska-Lakoma K, et al. Leiomyomatosis peritonealis disseminata of unusual course with malignant transformation: case report. Acta Obstet Gynecol Scand. 2015;94(2):220-3. doi: 10.1111/aogs.12549 [ Links ]
5. Julien C, Bourgouin S, Boudin L, Balandraud P. Disseminated peritoneal leiomyomatosis. J Gastrointest Surg. 2019;23(3):605- 7. doi: 10.1007/s11605-018-3841-7 [ Links ]
6. Mahmoud MS, Desai K, Nezhat FR. Leiomyomas beyond the uterus; benign metastasizing leiomyomatosis with paraaortic metastasizing endometriosis and intravenous leiomyomatosis: a case series and review of the literature. Arch Gynecol Obstet. 2015;291(1):223-30. doi: 10.1007/s00404-014-3356-8 [ Links ]
7. Barison GAS, Alvarenga-Bezerra V, Maranhão DDA, Gomes MTV. Tricky diagnosis and robot-laparoscopic surgical approach to disseminated peritoneal leiomyomatosis. J Minim Invasive Gynecol. 2021;28(9):1566-7. doi: 10.1016/j.jmig.2021.04.006 [ Links ]
8. Park BY, Leslie KO, Chen L, Vaszar LT, Cornella JL. A case of simultaneous benign metastasizing leiomyomas and disseminated peritoneal leiomyomatosis following endoscopic power morcellation for uterine disease. Female Pelvic Med Reconstr Surg. 2017;23(1):e1-3. doi: 10.1097/spv.0000000000000342 [ Links ]
9. Liu C, Chen B, Tang X, Xiong Y. Disseminated peritoneal leiomyomatosis after uterine artery embolization, laparoscopic surgery, and high intensity focused ultrasound for uterine fibroids: a case report. Int J Hyperthermia. 2020;37(1):925-8. doi: 10.1080/02656736.2020.1797909 [ Links ]
10. Anand N, Handler M, Khan A, Wagreich A, Calhoun S. Disseminated Peritoneal Leiomyomatosis Status Post Laparoscopic Hysterectomy with Morcellation. J Radiol Case Rep. 2016 Dec 31;10(12):12-8. doi: 10.3941/jrcr.v10i12.2904 [ Links ]
Comments (0)